Procesos energéticos del metabolismo. Redox y fosforilación
Las reacciones metabólicas son impulsadas por la energía química que proporcionan dos grupos de biomoléculas esesnciales en el metabolismo. Las reacciónes de oxidación-reducción y las de fosforilación-desforolización jugan un papel muy importante en la transferencia de energía en las reacciones metabólicas.
- Las coenzimas NADH, NADPH y FADH2, que suministran la energía de reducción-oxidación. Participan en las llamadas reacciones redox o de oxidación-reducción.
- Los nucleótidos trifosfato (ATP y en menor medida GTP), que almacenan energía en sus enlaces anhídrido fosfórico entre grupos fosfato. Participan en las reacciones de fosforilación-desfosforilación.

Reacciones de transferencia de electrones. Las reacciones redox
Una reacción de reducción-oxidación o redox es aquella en la que una molécula pierde electrones y se oxida, mientras que otra molécula gana electrones (los que perdió la primera molécula) y se reduce. Muchas de las reacciones y rutas metabólicas están basadas en intercambios de electrones entre moléculas.
La formación de cloruro de magnesio es un ejemplo de una reacción redox en la que sucede justo lo que acabamos de definir:
Mg + Cl2 → Mg2+ + 2Cl-
En esta reacción el átomo de magnesio pierde dos electrones, por lo que se oxida. Estos dos electrones los toma el cloro, que se reduce.
El fundamento de las reacciones de oxidación y reducción es la transferencia y/o acaparamiento de electrones. Sin embargo, en el contexto de la biología, muchas veces se puede utilizar un pequeña regla para averiguar a dónde van los electrones. En general:
- Si una molécula que contiene carbono gana átomos de H o pierde átomos de O durante una reacción, probablemente se ha reducido (ganó electrones).
- Por otro lado, si una molécula que contiene carbono pierde átomos de H o gana átomos de O, probablemente se ha oxidado (perdió electrones).
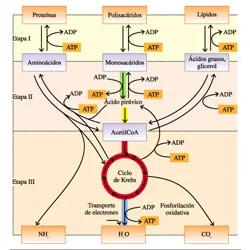
Ahora bien, ¿qué sentido tiene en el metabolismo estas reacciones de oxidación y reducción? ¿Por qué una célula se toma toda la molestia de extraer electrones de la glucosa, transferirlos a transportadores de electrones y pasarlos por una cadena de transporte de electrones en una larga serie de reacciones de reducción - oxidación? La respuesta básica es que todo esto tiene como fin el obtener energía de esa molécula de glucosa. La reacción básica de la degradación de glucosa es:
C6H12O6 + 6O2 → 6CO2 + 6H2O
ΔG = -686 kcal/mol
Esto es lo mismo que decir:
C6H12O6 + 6O2 → 6CO2 + 6H2O + energía
Los electrones están en un nivel de energía más alto cuando están en átomos menos electronegativos (como C o H) y en un nivel de energía más bajo cuando están en átomos más electronegativos (como el O). De esta forma, en una reacción como la degradación de la glucosa anterior, se libera energía porque los electrones se mueven a un nivel de energía más bajo, un estado más "cómodo", al pasar de la glucosa al oxígeno.

La energía que se libera cuando los electrones se mueven a un estado energético más bajo se puede capturar y usarse para realizar otros trabajos. En el proceso conocido como respiración celular, los electrones de la glucosa se mueven gradualmente a través de una cadena de transporte de electrones hacia el oxígeno, pasan a estados de energía cada vez más bajos y liberan energía en cada paso. El objetivo de la respiración celular es captar esta energía en forma de ATP.
En la célula, hay moléculas que se encargan de suministrar la energía de reducción-oxidación. Son los transportadores de electrones, unas pequeñas moléculas orgánicas que desempeñan un papel clave en el metabolismo celular. Su nombre es una buena descripción de su trabajo: recogen electrones de una molécula y los llevan a otra. Tres coenzimas son especialmente importantes en esta función:
- Nicotin adenin dinucleótido (abreviado NAD+ en su forma oxidada y NADH en su forma reducida). Es una coenzima que se halla en las células vivas y que está compuesta por un dinucleótido, es decir, por dos nucleótidos, unidos a través de grupos fosfatos: uno de ellos es una base de adenina y el otro, una nicotinamida.

Reacciones redox de dinucleótido de nicotinamida adenina NAD NADH - Nicotinamida adenina dinucleótido fosfato (abreviada NADP+ en su forma oxidada y NADPH2+ en su forma reducida). Es análogo del anterior.
- Flavín adenín dinucleótido (abreviado FAD en su forma oxidada y FADH2 en su forma reducida).

Reacciones redox de dinucleótido de nicotinamida adenina NAD NADH
Tanto el NADH como el NADPH son cofactores móviles, se trasladan de un enzima a otro; por el contrario, el FADH es un grupo prostético de las flavoproteínas, a las que están fuertemente unidas.
Las reacciones de oxidación de los sustratos orgánicos ocurren de modo acoplazo a la reducción de coenzimas oxidadas NAD+ y FAD, que se reducen y producen NADH y FADH2. Las reacciones de reducción requieren los electrones contenidos en las coenzimas reducidas NADH y FADH2.

Reacciones de fosforilación-desfosforilación
La energía liberada en las transferencias de electrones en la cadena de transporte de electrones se captura como un gradiente de protones, y es este gradiente del protones quien proporciona energía para la conversión de ADP a ATP mediante una enzima llamada ATP sintasa.
En otras palabras, la energía no se convierte en ATP, sino que parte de la energía liberada que se extrae en las reacciones redox se utiliza para unir ADP y fosfato inorgánico y así producir ATP. La energía se almacena en el enlace recién formado que está presente en el ATP pero no en el ADP.
Los nucléotidos trifosfato, entre los que destaca el ATP, almacenan una gran cantidad de energía en los enlaces anhídrido fosfórico que se establecen entre sus grupos fosfatos.
A un pH fisiológico, el ATP tiene cuatro cargas negativas. La repulsión eléctrica entre estas cargas del mismo signo es, en parte, responsable de la energía que se libera al hidrolizarse sus enlaces anhídrido fosfórico, pues la pérdida de un grupo fosfato disminuye la repulsión eléctrica intramolecular.
Por acoplamiento energético, la hidrólisis del ATP se utiliza en numerosas reacciones anabólicas que requieren energía.
La reacción contraria, es decir, la síntesis del ATP es energéticamente desfavorable. Las reservas de ATP en el organismo duran unos pocos segundos, por lo que se requiere su síntesis continua. Esto es posible gracias a la energía que aportan las reacciones catabólicas. Cualquier proceso que bloquee su producción provoca la muerte rápida.

Hashtags:
#metabolismo#anabolismo#catabolismo#enzima#autotrofo#heterotrofo#energia-libre#redox#fosforilacion#ruta-metabolica#celula
Juan Luis Menéndez
Me gusta la divulgación de la naturaleza y el patrimonio cultural, motivos por los que he decidido comenzar el desarrollo de asturnatura.com. Soy un amante de la botánica y la geología.
Comparte en:
Índice:
- Concepto de metabolismo. Catabolismo y anabolismo
- Organismos autótrofos y heterótrofos
- Características de las rutas metabólicas
- La energía libre en las rutas metabólicas
- Procesos energéticos del metabolismo. Redox y fosforilación
- Las enzimas
- El ATP
- Regulación del metabolismo
Más populares en Bioquímica:
 Fases de la Meiosis
Fases de la Meiosis Los monosacáridos
Los monosacáridosPalabras clave:
Artículos similares
Citar como
Menéndez Valderrey, Juan Luis. "Procesos energéticos del metabolismo. Redox y fosforilación". asturnatura.com [en línea] Num. 853, 02/08/2021 [consultado el 15/4/2025]. Disponible en https://www.asturnatura.com.
ISSN 1887-5068